BioS+
-
바이오젠, ‘타우 ASO’ AD 2상 “혼재 불구, 3상 진행”
이주연 기자 2026-05-15 12:01
-
큐로셀, 림카토 "9월 급여출시 기대..내년 2차 3상 추진"
김성민 기자 2026-05-15 11:56
-
HLB 엘레바, 'FGFR2 저해제' 담관암 後 "다음 스텝은?"
이효빈 기자 2026-05-15 10:34
-
노보노, '위고비HD' 3상 조기반응자 “72주차 28%감량"
이효빈 기자 2026-05-15 06:35
-
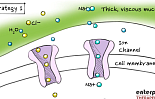
엔터프라이즈, 버텍스 실패 ‘ENaC 차단제’ CF 2상 “효능”
신창민 기자 2026-05-14 14:07
-
온코닉, 'PARP/TNKS' PARP내성 모델서 효과 "논문"
이주연 기자 2026-05-14 12:24
-
'AI설계' 갤럭스, ‘PD-1xIL-18v' 초기결과 "AACR 발표"
샌디에고(미국)=이주연 기자 2026-05-14 10:15
-
베링거, 이뮤니타스 ‘염증세포 사멸’ 항체 "4억€ 딜"
신창민 기자 2026-05-14 09:06
-
‘알파폴드’ 아이소모픽, 시리즈B 21억弗 “역대급 펀딩”
이효빈 기자 2026-05-14 06:24
-
마카리 FDA 국장 사임..대행에 '디아만타스' 부국장
이주연 기자 2026-05-13 14:18
-
키베르나, ‘CD19 CAR-T’ 자가면역 첫 美허가신청 “시작”
신창민 기자 2026-05-13 12:07
-
‘세포치료제 철수’ 노보노, 파킨슨병 줄기세포도 “매각”
신창민 기자 2026-05-13 11:21
-
'최초 PROTAC' 리겔 품으로..계약금 불과 8500만弗
김성민 기자 2026-05-13 09:46
-
BMS, 中항서와 ‘13개 파이프라인’ 152억弗 “빅딜”
이주연 기자 2026-05-13 08:34
-
마드리갈 "경쟁 GLP-1 불구", 'MASH' 매출 127% 급증
김성민 기자 2026-05-13 06:41
-
프랙틸, 첫 'GLP-1 AAV' 네덜란드서 당뇨병 “임상 승인”
신창민 기자 2026-05-12 19:39