국제
-
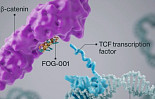
파라빌리스, 시리즈F 3.05억弗.."Wnt 타깃 펩타이드"
이주연 기자 2026-01-12 15:58
-
에피바이오, 시리즈B 1.07억弗..EGFR ‘이중항체 TPD’
신창민 기자 2026-01-12 09:25
-
릴리, '젭바운드+IL-17' 건선성관절염 3b상도 "성공"
이주연 기자 2026-01-12 07:24
-
알베우스, 비만 "분기투여" 'MariTide 전략' 1.6억弗 출범
김성민 기자 2026-01-09 12:46
-
GSK, ‘HBV ASO’ 만성B형간염 완치 3상 “히트”
신창민 기자 2026-01-09 09:58
-
알루미스, ‘TYK2 저해제' 건선 3상 "성공”..주가 115%↑
이주연 기자 2026-01-09 09:08
-
릴리, 벤틱스 12억弗 인수..'경구 NLRP3 저해제' 확보
이주연 기자 2026-01-08 14:48
-
릴리, 'AI' 님버스와 13.55억弗 추가 딜.."경구 비만약"
이주연 기자 2026-01-08 06:45
-
화이자, 카토그래피와 ‘암항원 발굴’ 8.5억弗 옵션딜
신창민 기자 2026-01-07 14:00
-
제나스, ‘이중타깃 항체’ 자가면역 3상 “기대 이하”
신창민 기자 2026-01-07 10:48
-
인실리코, 세르비에와 '항암제 AI발굴' 8.88억弗 딜
이주연 기자 2026-01-07 08:50
-
이노벤트, 'CTLA-4' 결장암 수술전요법 "첫" 中승인
이주연 기자 2026-01-06 10:16
-
울트라제닉스, ‘SOST 항체’ 골형성부전증 3상 “실패”
신창민 기자 2026-01-05 13:57
-
'릴리 AI 파트너' 인실리코, 홍콩 IPO서 "2.93억弗 조달"
김성민 기자 2026-01-05 09:11
-
애브비, 中서 ‘DLL3xCD3’ 삼중 TCE 12억弗 옵션딜
이주연 기자 2026-01-05 06:14
-
바이오헤븐, '칼륨채널 활성제' 우울증 2상 "실패"
이주연 기자 2026-01-02 11:00