전체기사
-
프로바이오, 큐로셀 ‘림카토’ 시판허가에 “핵심 지원”
신창민 기자 2026-05-11 16:01
-
할로자임, GSK와 'ADC SC’ 파트너십 딜..”ADC 첫계약”
이효빈 기자 2026-05-11 15:53
-
프로티나, 'SOX9 활성 저분자' 경쟁력 "학회 업데이트"
김성민 기자 2026-05-11 15:13
-
GC셀 美관계사 아티바, 'NK세포' 자가면역 임상 “긍정적”
이효빈 기자 2026-05-11 13:48
-
에자이, '레켐비SC' AD 시작치료 FDA심사 “3개월 연장”
신창민 기자 2026-05-11 11:45
-
지놈앤컴퍼니, 'ITGB4xTROP2 ADC' AACR서 "첫 공개"
샌디에고(미국)=이주연 기자 2026-05-11 10:54
-
어센디스, ‘지속형 IL-2’ 개발 '중단' "전략적 판단"
신창민 기자 2026-05-11 10:38
-
셀센트릭, 시리즈D 2.2억弗..'p300/CBP 경구제' MM 3상
이주연 기자 2026-05-11 10:25
-
온코닉, 1Q 매출 229억 "전년比 151% 증가"
이주연 기자 2026-05-11 10:22
-
스파크바이오, pre-IPO 315억.."코스닥 IPO 본격화"
김성민 기자 2026-05-11 09:28
-
큐라클-맵틱스, 'Tie2xVEGF' 美메멘토에 총 10.7억弗 L/O
김성민 기자 2026-05-11 09:09
-
삼진제약, ‘에필라탐 서방정 1000mg’ 국내 단독출시
이효빈 기자 2026-05-11 09:01
-
伊안젤리니, 카탈리스트 41억弗 인수.."뇌질환 강화"
이주연 기자 2026-05-11 08:52
-
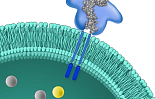
알테오젠, ‘장기지속형’ 플랫폼 기반 ”비만치료제 개발”
이효빈 기자 2026-05-11 06:03
-
GC녹십자, 1분기 매출 4355억 "전년比 13.5% 증가"
이효빈 기자 2026-05-08 17:13
-
대웅제약, 티온랩과 '월1회 GLP-1' 비만치료제 개발
이효빈 기자 2026-05-08 16:19