국제
-
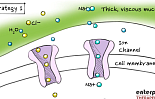
엔터프라이즈, 버텍스 실패 ‘ENaC 차단제’ CF 2상 “효능”
신창민 기자 2026-05-14 14:07
-
베링거, 이뮤니타스 ‘염증세포 사멸’ 항체 "4억€ 딜"
신창민 기자 2026-05-14 09:06
-
마카리 FDA 국장 사임..대행에 '디아만타스' 부국장
이주연 기자 2026-05-13 14:18
-
"머크, 할로자임 'MDASE 특허' 심판(PGR)서 무효 판단"
김성민 기자 2026-05-13 12:26
-
키베르나, ‘CD19 CAR-T’ 자가면역 첫 美허가신청 “시작”
신창민 기자 2026-05-13 12:07
-
‘세포치료제 철수’ 노보노, 파킨슨병 줄기세포도 “매각”
신창민 기자 2026-05-13 11:21
-
'최초 PROTAC' 리겔 품으로..계약금 불과 8500만弗
김성민 기자 2026-05-13 09:46
-
BMS, 中항서와 ‘13개 파이프라인’ 152억弗 “빅딜”
이주연 기자 2026-05-13 08:34
-
프랙틸, 첫 'GLP-1 AAV' 네덜란드서 당뇨병 “임상 승인”
신창민 기자 2026-05-12 19:39
-
인히브릭스, ‘OX40+키트루다’ 직접비교 2상 “히트”
신창민 기자 2026-05-12 13:48
-
엔트라다, ‘펩타이드 접합 ASO’ DMD 1/2상 “기대 이하”
신창민 기자 2026-05-12 10:52
-
'나스닥 재도전' 오디세이, 2.79억弗 IPO.."RIPK2 임상"
이효빈 기자 2026-05-12 09:00
-
마카리 FDA 국장 '해임계획'에 "트럼프 서명" 보도
이주연 기자 2026-05-11 16:05
-
GC셀 美관계사 아티바, 'NK세포' 자가면역 임상 “긍정적”
이효빈 기자 2026-05-11 13:48
-
에자이, '레켐비SC' AD 시작치료 FDA심사 “3개월 연장”
신창민 기자 2026-05-11 11:45
-
어센디스, ‘지속형 IL-2’ 개발 '중단' "전략적 판단"
신창민 기자 2026-05-11 10:38