전체기사
-
지아이바이옴, ‘마이크로바이옴’ 대장암 후유증 IND 승인
신창민 기자 2025-05-08 10:49
-
릴리, 'ALS 항체' 발굴 파트너 알케맙서 4.15억弗 L/I
정지윤 기자 2025-05-08 10:19
-
GC셀, 자가면역 ‘CD19 CAR-NK’ 범부처 과제 선정
신창민 기자 2025-05-08 10:08
-
HK이노엔, 'cAMP 편향 GLP-1' 비만 "국내3상 IND 승인"
김성민 기자 2025-05-08 09:54
-
온코닉, ‘PARP/TNKS 저해제’ 임상 2건 “ASCO 발표”
신창민 기자 2025-05-08 09:29
-
J&J, ‘메이라 인수’ AAV 희귀 안과질환 3상 "실패"
이주연 기자 2025-05-08 09:28
-
에이비엘, 'B7-H4x4-1BB' 키트루다 병용 "전임상 공개"
시카고(미국)=김성민 기자 2025-05-08 08:28
-
대웅제약, 면역항암 ‘ARG 저해제’ 전임상 “첫 공개”
시카고(미국)=신창민 기자 2025-05-08 07:18
-
차바이오 마티카, 美 A&M대와 'CGT 연구개발' 협약
김성민 기자 2025-05-07 15:27
-
아비나스, 화이자 'PROTAC' 3상 '철회'..인력 33% 해고
김성민 기자 2025-05-07 14:23
-
버텍스, ‘AAV 유전자치료제’ 프로그램 “전면 중단”
신창민 기자 2025-05-07 13:45
-
FDA ‘CBER’ 막스 후임에 '비나이 프라사드' 소장 임명
이주연 기자 2025-05-07 12:04
-
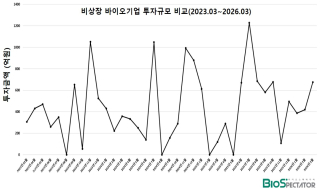
4월 비상장 바이오투자, '3월이어 또 1곳'..290억 "TPD"
정지윤 기자 2025-05-07 11:52
-
SK바사, '조류독감 백신' 개발 "질병청 사업선정"
정지윤 기자 2025-05-07 10:43
-
온코닉, 스웨덴 제약사와 ‘자큐보’ 판매계약 체결
신창민 기자 2025-05-07 10:23
-
티움바이오, 'GnRH 길항제' 자궁근종 2상 "주요지표 충족"
정지윤 기자 2025-05-07 10:13