전체기사
-
HLB, ‘리보세라닙 병용’ 간암 “FDA 허가 재신청 완료”
신창민 기자 2026-01-26 08:51
-
퍼스트바이오, 시리즈D 317억 유치 "리가켐 SI 참여"
김성민 기자 2026-01-26 08:40
-
BMS, 자눅스와 ‘masking’ 항암제 개발 “8억弗 딜”
신창민 기자 2026-01-26 06:30
-
인실리코, 'NLRP3 저해제’ 권리50% "6600만弗 L/O"
이효빈 기자 2026-01-23 14:54
-
에스티팜, ‘올리고핵산’ 원료 공급 “5600만弗 계약”
신창민 기자 2026-01-23 14:53
-
씨어스테크놀로지, 26일 홍콩서 "해외 NDR 진행"
김성민 기자 2026-01-23 14:52
-
노보노, 중단 ‘당뇨병 세포치료제’ 애스펙트에 "매각"
이주연 기자 2026-01-23 13:01
-
FDA, MM서 ‘MRD 가속승인’ 가이드라인 “초안 발표”
신창민 기자 2026-01-23 10:45
-
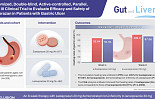
온코닉, P-CAB ‘자큐보’ 위궤양 3상 “논문 게재”
이주연 기자 2026-01-23 10:20
-
에이비엘바이오, 홍콩·싱가포르서 "해외 NDR 진행"
김성민 기자 2026-01-23 10:12
-
대웅제약, 강북구 신일병원에 스마트병동 '씽크' 공급
김성민 기자 2026-01-23 10:02
-
코르부스, ‘ITK 저해제’ 아토피 1상 "성공"..주가 175%↑
이주연 기자 2026-01-23 09:06
-
J&J, 올 매출 1000억弗 전망..'항암 1위' 빅파마 목표
김성민 기자 2026-01-23 06:10
-
HLB생명과학, 157억 규모 EB 발행 결정
신창민 기자 2026-01-22 17:24
-
디아고날, 시리즈B 1.25억弗..'클러스터링 항체' 임상
이효빈 기자 2026-01-22 13:49
-
Vetter파마, '지속가능성 최고등급·배출량 감축' 인증
이주연 기자 2026-01-22 12:00