검색
검색어를 입력하세요.
-
디앤디파마텍, 코스닥 기술성평가 'A, A' 통과
김성민 기자 2021-09-27 19:01
-
펩트론, 호주 인벡스와 'IIH 치료제' 생산공급계약
노신영 기자 2021-09-27 13:42
-
카프리코, ‘동종유래 CDC’ DMD 2상 “증상 71%지연”
서윤석 기자 2021-09-27 12:45
-
디앤디파마텍, ‘GLP-1/GCG 작용제' 中살루브리스에 L/O
서윤석 기자 2021-09-27 11:18
-
애니메디솔루션, 코스닥 기술성평가 통과 'A, A'
윤소영 기자 2021-09-27 10:51
-
JW크레아젠, 온코인사이트와 ‘CAR-M’ 공동개발 MOU
노신영 기자 2021-09-27 10:37
-
압타머사이언스, BBB 투과 'TfR 압타머' 플랫폼 "발표"
김성민 기자 2021-09-27 10:02
-
ENGAIN targets “Global medical devices” with “Polymer treatment agent”
Shinyoung Roh 기자 2021-09-27 09:51
-
인벤티지랩, 탈모치료 '지속형 주사제’ 호주 1상 승인
서윤석 기자 2021-09-27 09:50
-
노바티스, '안과 AAV' 아크토스 인수.."IRD∙AMD 타깃"
노신영 기자 2021-09-27 08:46
-
AZ, saRNA '백스에쿼티'와 딜.."Next mRNA 도전"
서윤석 기자 2021-09-27 06:23
-
화이자, 코로나19백신 3차 "고위험군" FDA 긴급승인
서일 기자 2021-09-24 14:13
-
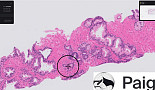
페이지, 전립선암 'AI 병리진단' "FDA 최초 승인"
서윤석 기자 2021-09-24 13:37
-
일동홀딩스, 일동바이오사이언스 지분 200억 매각
노신영 기자 2021-09-24 11:49
-
Seagen-젠맙, '최초' 자궁경부암 ADC "FDA 가속승인"
차대근 기자 2021-09-24 11:03