검색
검색어를 입력하세요.
-
셀트리온, '고농도 휴미라 시밀러' 캐나다 “판매허가”
서윤석 기자 2021-12-30 10:24
-
[인사]종근당, 계열사 임원인사
서윤석 기자 2021-12-30 09:29
-
[새책]봄을 기다리며..『바이오스펙테이터 연감 2022』
서일 기자 2021-12-30 09:26
-
퀴델, '체외진단' 올소 60억弗 인수..글로벌 7위 올라
윤소영 기자 2021-12-29 14:26
-
[인사]HK콜마, inno.N 곽달원 대표 등 사장단인사
김성민 기자 2021-12-29 12:20
-
손성향 교수팀, 박테리아 3종 혼합균 “IBD 개선효능”
노신영 기자 2021-12-29 11:20
-
모더나, 한국정부와 '코로나백신' "2천만회분 공급계약"
김성민 기자 2021-12-29 09:52
-
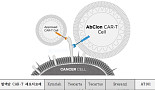
앱클론, CD19 CAR-T 국내 1/2상 "IND 승인"
김성민 기자 2021-12-29 09:28
-
美브릿지, ATTR 심근병증 3상 "실패"..주가 72%↓
서일 기자 2021-12-29 08:01
-
이오플로우, 자이힙과 웨어러블 '비만·NASH' "JV 설립"
김성민 기자 2021-12-28 16:27
-
김용삼 생명硏, '1/3 크기' 초소형 CRISPR "4가지 특징"
김성민 기자 2021-12-28 13:47
-
코오롱티슈진, '인보사' 골관절염 미국 3상 투약재개
윤소영 기자 2021-12-28 11:27
-
휴이노, 시리즈C 435억 유치.."유한 SI참여, 2대주주"
윤소영 기자 2021-12-28 10:50
-
휴온스바이오, '보툴리눔 톡신' 미간주름 2상 승인
윤소영 기자 2021-12-28 10:00
-
노바티스, RNAi '렉비오' "드디어" 美시판..상업화 숙제
김성민 기자 2021-12-28 09:53
![[인사]종근당, 계열사 임원인사](https://img.etoday.co.kr/crop/155/90/1643436.jpg)
![[새책]봄을 기다리며..『바이오스펙테이터 연감 2022』](https://img.etoday.co.kr/crop/155/90/1703057.jpg)

![[인사]HK콜마, inno.N 곽달원 대표 등 사장단인사](https://img.etoday.co.kr/crop/155/90/1702582.jpg)