검색
검색어를 입력하세요.
-
일동제약 "올해 혁신적 성과창출..신약 연구속도↑"
장종원 기자 2020-01-02 13:45
-
한미약품 "2020년 '새로운 도전'으로 제약강국 열자"
장종원 기자 2020-01-02 13:35
-
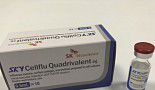
SK바이오사이언스, 4가 독감백신 첫 'WHO PQ' 인증
장종원 기자 2020-01-02 13:35
-
스펙트럼 '포지오티닙', 앞으로 남아있는 임상발표는?
김성민 기자 2020-01-02 11:46
-
Peptron, Two-track Strategy for Clinical Trial of ‘PT320’ Targeting Parkinson’s Disease
Sungmin Kim 기자 2020-01-02 11:27
-
대웅제약 "2020년 혁신신약 성과창출 원년될 것"
장종원 기자 2020-01-02 11:27
-
보령제약 "과감한 투자로 '제2의 바이젠셀' 발굴"
장종원 기자 2020-01-02 11:10
-
KIST, 뉴로바이오젠에 척수손상·뇌졸중 치료제 기술이전
김성민 기자 2020-01-02 10:34
-
에이치엘비생명과학, 한용해 바이오사업부 사장 선임
장종원 기자 2020-01-02 09:55
-
휴온스, 제네릭 국소마취주사제 美 허가
장종원 기자 2020-01-02 09:54
-
'2020 상장예고' 바이오기업 30곳↑..문턱 높아진다
장종원 기자 2020-01-02 06:46
-
2019 빅파마 '빅딜 10개'로 본 M&A 트렌드
김성민 기자 2020-01-01 09:00
-
대웅제약, 나보타 中 3상 착수..2022년 발매 목표
장종원 기자 2019-12-31 10:46
-
'2020 충북 바이오프로그램 통합설명회' 개최
장종원 기자 2019-12-31 10:17
-
PARP 저해제 '린파자', 췌장암까지 'FDA 승인'
김성민 기자 2019-12-31 09:21